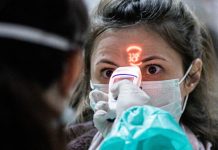
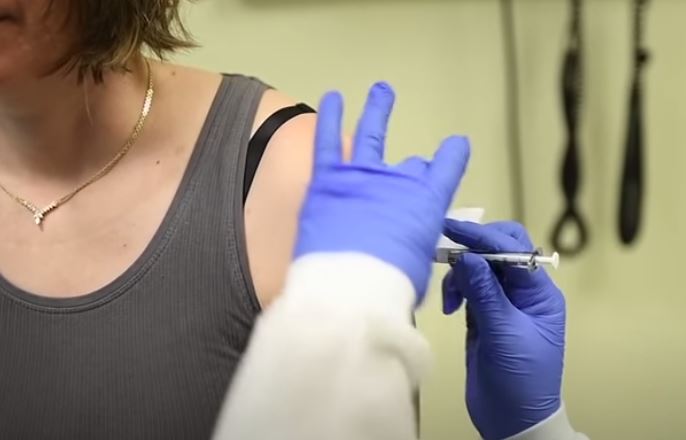
La compañía de biotecnología Moderna inició este 27 de julio la fase 3 de ensayos clínicos en 30.000 voluntarios para probar la eficacia y seguridad de su posible vacuna contra el Covid-19, la primera de EE. UU. en pasar a esa promisoria etapa.
En Estados Unidos se da inicio a la tercera fase de ensayos de una posible vacuna en contra el Covid-19. La investigación, que es desarrollada por la compañía Moderna y dirigida por el Instituto Nacional de Alergias y Enfermedades Infecciosas, tiene como objetivo evaluar la efectividad y seguridad del fármaco «a gran escala», por lo que se probará en más de 30.000 voluntarios.
El estudio también busca responder si la vacuna puede prevenir la muerte causada por el nuevo coronavirus y si solo una dosis puede prevenir la enfermedad sintomática, según anuncia un comunicado de la compañía.
«Somos optimistas, cautelosamente optimistas» de que la vacuna funcionará y que «hacia el final del año» habrá datos que lo demuestren, dijo el doctor Stephen Hoge, presidente de Moderna, a un subcomité de la Cámara de Representantes de EE. UU.
Este es el primer estudio cobijado por el Gobierno de Estados Unidos que logra llegar a una fase «avanzada», luego de que Washington urgiera a los investigadores a acelerar el desarrollo de fármacos que ayuden a contrarrestar los efectos del nuevo coronavirus en la población.
A fecha de 26 de julio, en Estados Unidos, el país más afectado por la pandemia, los casos de Covid-19 ascendieron a 4,18 millones con más de 146.000 muertes, de acuerdo a las cifras reportadas por la Universidad Johns Hopkins. En las últimas cuatro jornadas se han registrado récords de 1.000 fallecimientos diarios.
Así se llevarán a cabo las pruebas en la fase 3 de ensayos en humanos
Según explicó Moderna, en este ensayo se contará con la colaboración voluntaria de 30.000 participantes, quienes en un plazo de 28 días recibirán aleatoriamente dos dosis de la vacuna, la mRNA-1273, o dos dosis de placebo de solución salina.
Ni los doctores ni los participantes sabrán quién está asignado a qué grupo, únicamente los investigadores tendrán conocimiento de la administración real de la posible vacuna a cada participante.
Los resultados obtenidos en la fase 2, publicados a principios de este mes, mostraron que los voluntarios que recibieron dos dosis de la vacuna de Moderna tenían altos niveles de anticuerpos que excedían los niveles promedio observados en personas que se habían recuperado de la enfermedad.
A pesar de las buenas noticias y de estar en la última etapa de desarrollo previo a una posible distribución masiva, los científicos también han advertido que el producto final todavía podría tardar varios meses.
«Tener una vacuna segura y efectiva distribuida para fines de 2020 es una meta difícil, pero es la meta correcta para el pueblo estadounidense», dijo el director del Instituto Nacional de Salud, Francis Collins.
Según la Organización Mundial de la Salud, actualmente en el planeta se están desarrollando más de 150 posibles vacunas contra el coronavirus que se encuentran en diversas etapas de desarrollo. 23 de esos proyectos ya realizan ensayos en humanos, entre estos, el fármaco de Moderna es uno de los cuatro más avanzados.
Dos vacunas fabricadas en China y otra desarrollada por la Universidad de Oxford en conjunto con la compañía británica-sueca AstraZeneca, en Reino Unido, también comenzaron a hacer pruebas de fase 3 en decenas de miles de personas.
Algunas de estas investigaciones se llevan a cabo en Brasil, Sudáfrica, EE. UU. y otros países fuertemente afectados por la pandemia pero en una cantidad mucho menor de pacientes; por lo que los expertos aseguran que el estudio de Moderna es, hasta ahora, el más extenso no solo en cantidad de voluntarios sino a nivel de presupuesto.
Moderna logra doblar la financiación para su vacuna
En su comunicado, Moderna también señaló que ha modificado su contrato con la Autoridad de Investigación y Desarrollo Avanzado Biomédico (BARDA, por sus siglas en inglés) para que amplíe en 472 millones de dólares la cantidad inicial que iba a destinar al desarrollo de la vacuna mRNA-1273, lo que asegura un presupuesto total de unos 955 millones de dólares.
El contrato original con el organismo para el desarrollo de la vacuna proveía a la compañía de 483 millones, que originalmente iba a tener un «número más pequeño de participantes en la tercera fase» en comparación con los 30.000 voluntarios que necesitará ahora.
Moderna dijo que mantiene sus planes de administrar aproximadamente 500 millones de dosis al año, y posiblemente hasta 1.000 millones de dosis al año, a partir de 2021. La noticia de los avances en el estudio aumentó las acciones de Moderna en más de un 8 % antes del toque de campana en Wall Street este 27 de julio.